top of page
盧創
工作室


讓創意落地,發揮影響力
將深度科學、商業洞察與職涯策略,轉化為清楚且可執行的下一步。

學術研究與心得
實驗室生活紀錄、研究思路與學界產業的連結。


In Vivo CAR-T 自體免疫療法:開創免疫治療新前沿
In Vivo CAR-T 自體免疫療法:在體內重塑免疫系統 前言 CAR-T 療法已徹底改變血液腫瘤治療格局。然而,其拓展至自體免疫疾病的應用,仍受限於高昂成本、製程複雜度,以及難以規模化生產等挑戰。 如今,一種新的典範正在形成: in vivo CAR-T 自體免疫療法 。 不同於將 T 細胞取出體外改造、培養數週後再回輸體內,in vivo 策略是在患者體內直接編程免疫細胞,使人體本身成為製造場域。 對於自體免疫疾病而言——其治療目標是「免疫重置」而非腫瘤清除——這種差異可能具有決定性意義。 什麼是 In Vivo CAR-T? 傳統(ex vivo)CAR-T 療法流程包括: 白血球分離術(Leukapheresis) 病毒載體基因轉殖 細胞體外擴增 品質控制檢測 回輸患者體內 相較之下, in vivo CAR-T 自體免疫療法 是透過病毒載體或標靶奈米顆粒,將編碼 CAR 的遺傳物質(mRNA 或 DNA)直接送入體內循環中的 T 細胞。 這種概念轉變看似簡單,卻極具顛覆性: 從體外製造細胞 轉向在體內重新編程免疫系統。 這使 CAR

Jason Lu
2天前讀畢需時 6 分鐘


ADC 系列(七)Next-Generation ADC Platforms:下一代抗體藥物偶聯體正在如何被設計?
Executive Summary 抗體藥物偶聯體(ADC)在過去十年已成為腫瘤治療的重要藥物類型。 然而,第一代與第二代 ADC 的設計仍然存在限制,例如: 單一 payload 機制 單一 target 分子工程彈性有限 因此,許多研究團隊開始重新思考: 如果 ADC 不只是「抗體+毒藥」,而是一個可工程化的平台呢? 這篇文章將介紹 next-generation ADC platforms 的主要方向,包括: dual-payload ADC bispecific ADC payload engineering tumor-selective linker design targeted delivery platforms 這些新策略正在重新定義 ADC 的未來。 一、為什麼需要 Next-Generation ADC? 早期 ADC 的設計通常比較簡單: 單一 monoclonal antibody 單一 payload 傳統 linker 然而腫瘤生物學的複雜性意味著: tumor heterogeneity adaptive re

Jason Lu
3月15日讀畢需時 2 分鐘


mRNA-LNP Stability:RNA藥物成功背後最困難的工程挑戰
前言 在 COVID-19 疫苗成功之後, mRNA 技術迅速成為生醫領域最重要的藥物平台之一 。 透過讓人體細胞暫時表達特定蛋白質,mRNA therapeutics 正被應用於多種醫療領域,例如: 疫苗 癌症免疫治療 蛋白質替代療法 基因編輯(CRISPR delivery) 然而,mRNA 本身極其脆弱。 如果沒有保護機制,mRNA 在體內幾乎會在短時間內被降解。因此所有 mRNA 藥物都依賴一種關鍵技術: Lipid Nanoparticles (LNPs) 。 這些奈米顆粒能夠包覆 RNA,並將其安全地送入細胞。 但這項技術同時帶來了一個巨大的挑戰: mRNA-LNP 的穩定性非常複雜。 近期一項研究系統性分析了不同配方與儲存條件對 mRNA-LNP 長期穩定性的影響,並揭示了影響 RNA 藥物 shelf-life 的關鍵因素。 mRNA- LNP 的基本結構 要理解為什麼 mRNA-LNP stability 如此具有挑戰性,我們需要先了解這種奈米遞送系統的基本組成。 典型的 mRNA-LNP 由四種主要脂質組成: Ioniz

Jason Lu
3月14日讀畢需時 5 分鐘


ADC 系列(六)ADC Combination Therapy:為什麼抗體藥物偶聯體幾乎都需要合併療法?
Executive Summary 抗體藥物偶聯體(Antibody–Drug Conjugates, ADCs)在過去十年間已成為腫瘤藥物開發的重要平台。然而,即使是臨床上表現非常成功的 ADC,也很少能長期單獨控制腫瘤。 原因在於腫瘤具有高度適應能力。腫瘤細胞可以透過多種機制逐漸逃避 ADC 的攻擊,例如抗原下降、內吞效率改變、或 DNA repair pathway 的補償。 因此,越來越多研究開始探索 ADC combination therapy ,也就是將 ADC 與其他抗癌策略結合,例如免疫療法、小分子標靶藥物或 DNA repair 抑制劑。 這篇文章將解析: 為什麼單一 ADC 很難長期控制腫瘤 ADC 與免疫療法的機制協同 ADC 與 DNA repair 抑制劑的潛在組合 Multispecific ADC 的未來方向 Combination therapy 的臨床試驗 landscape 理解這些概念,有助於從單一藥物開發轉向 平台級策略設計 。 一、為什麼單一 ADC 很難長期控制腫瘤? 在前一篇文章中,我們討論了 AD

Jason Lu
3月7日讀畢需時 4 分鐘


ADC 系列(五)ADC Resistance:為什麼抗體藥物偶聯體會失效?
文章定位 這是 ADC 系列第五篇。 在前幾篇中,我們談了: ADC 系統設計 Linker 與 conjugation Target selection 臨床轉譯與產業價值 這一篇要面對一個更現實的問題: 即使設計合理、臨床成功,為什麼 ADC resistance 仍然不可避免? Executive Summary ADC resistance 是多機制共同作用的結果。 抗原下降與異質性會降低藥物進入效率。 Internalization 與 lysosomal trafficking 改變會減少 payload 釋放。 ABC transporters 可能將 payload 排出細胞。 DNA damage response 與細胞適應機制降低毒性效果。 下一代 ADC 正透過 dual payload、multispecific 與新機制 payload 來延緩抗藥性。 一、Target Downregulation 與抗原異質性 最直觀的 ADC resistance 機制是: 抗原表現下降 抗原基因變異 腫瘤內部高度異質性 當抗原密

Jason Lu
2月22日讀畢需時 3 分鐘


ADC 系列(四)ADC Target Selection:哪些抗原真正適合抗體藥物偶聯體?
前言 這是 ADC 系列的第四篇文章。 如果前幾篇我們談的是: ADC 是一個整合系統(Series 一) 為什麼 2020 年後 ADC 進入成熟期(Series 二) Linker 與 Conjugation 的工程核心(Series 三) 那麼這一篇將往更上游走一步,回答一個根本問題: ADC target selection:哪些抗原真的適合做 ADC? 這篇文章寫給沒有 ADC 背景,但希望從第一原理理解「生物學條件如何決定藥物上限」的讀者。 Executive Summary | ADC target selection ADC target selection 是整個專案的第一個、也是最難修正的決策。 高表現抗原不等於適合 ADC,internalization 才是關鍵。 抗原密度、腫瘤異質性與正常組織表現,直接決定療效與毒性風險。 Antigen shedding 可能成為隱性藥物黑洞(antigen sink)。 Multispecific ADC 提供新方向,但同時提高設計門檻。 一、ADC 為什麼不是所有腫瘤標的的萬用解?

Jason Lu
2月14日讀畢需時 4 分鐘


LNPDB是什麼?從資料庫到 AI 與分子動力學,重新理解脂質奈米粒的設計邏輯
前言 為什麼 LNP 領域,一直缺一個「PDB 等級」的資料庫? 如果你實際參與過 mRNA、siRNA 或 CRISPR 的 lipid nanoparticle(LNP)設計,你很可能有這樣的感覺: 我們其實做了非常多 LNP screening,但這些資料始終無法真正「累積成知識」。 LNP 領域長期存在一個結構性的問題: 資料很多,但高度分散;實驗成功,但難以歸納。 不同研究使用不同配方、不同 readout、不同實驗條件,使得資料難以跨研究比較或重複使用。 與蛋白質工程不同,LNP 設計至今沒有一個像 Protein Data Bank(PDB) 那樣的中央化基礎建設,能夠系統性整理「結構 × 配方 × 功能」之間的關係。這也直接限制了 AI 模型與理性化設計的發展。 LNPDB 是什麼?Lipid Nanoparticle Database 作為公共資料基礎建設 Lipid Nanoparticle Database(LNPDB) https://lnpdb.molcube.com/ LNPDB 是由 MIT(Dr. Daniel

Jason Lu
2月8日讀畢需時 3 分鐘


ADC 系列(三)Linker 與 Conjugation:ADC 真正的工程核心,為什麼多數團隊低估了它?
前言 這是 ADC 系列的第三篇文章,寫給 沒有化學或 ADC 工程背景 ,但想真正理解: 為什麼很多 ADC 專案「看起來都合理」,最後卻在臨床或放大製程中失敗? 本篇將聚焦在 linker 與 conjugation strategy —— 這兩個最常被視為「技術細節」,卻最常成為 結構性失敗來源 的關鍵設計。 Executive Summary 如果你只記得一件事: ADC 的成敗,往往不是輸在抗體或 payload,而是輸在 linker 與偶聯策略。 因為 linker 與 conjugation 決定的不是「藥有多毒」, 而是: 毒藥什麼時候釋放 在哪裡釋放 有多少分子真的能照設計行事 一、為什麼 Linker 是 ADC 最被低估的元件? 在許多入門介紹中,linker 常被一句話帶過: 「linker 是把抗體和藥物接起來的化學結構。」 但在實際開發中,linker 解決的是一個 極度困難的工程問題 : 如何讓 ADC 在血液中穩定數天,卻能在癌細胞內準確釋放 payload? 這意味著 linker 必須同時滿足三個互相衝突的

Jason Lu
2月7日讀畢需時 4 分鐘


ADC 系列(二)為什麼現在的 ADC,和 10 年前完全不一樣?──從失敗中進化的抗體藥物偶聯體(ADC Evolution)
這是 ADC 系列的第二篇文章,寫給 沒有 ADC 專業背景 、但想理解 ADC evolution(抗體藥物偶聯體的演進) 的讀者。本篇聚焦於 why ADCs failed before, and why next-generation ADCs succeed today ,從歷史失敗、工程修正到平台策略,系統性解析不同 ADC generations 之間的關鍵差異。 Executive Summary 如果你只記得一件事: ADC 並不是突然變強,而是花了十多年,逐步修正那些「一開始就會失敗的設計」。 今天成功的 ADC,看起來像是技術突破,實際上是大量失敗後,慢慢形成的工程與策略共識。 一、 回到起點:為什麼早期 ADC 失敗率這麼高?(Early ADC Development) 回顧 ADC evolution 的歷程可以發現,抗體藥物偶聯體並不是突然變成熟,而是經歷了多個世代的失敗與修正,才逐步形成今天被稱為 next-generation ADC platform 的設計邏輯。 在 2000–2010 年間,ADC 被

Jason Lu
2月1日讀畢需時 4 分鐘


沒有生物系背景,我怎麼自學分子生物學?
前言 在跨領域學習的路上, 分子生物學幾乎是所有非生物本科背景的第一道高牆 。 對工程背景的人來說,困難通常不在於「不努力」,而在於: 名詞太多、關係太複雜 不知道哪些一定要懂,哪些可以先放下 學了卻不知道怎麼用 這篇文章,我想很誠實地分享: 沒有生物系背景,我是怎麼自學分子生物學的。 為什麼分子生物學是跨領域學習中最不能跳過的一關 很多人會問:「我真的需要學分子生物學嗎?」 我的答案通常是: 如果你想長期待在生醫領域,是的。 原因很簡單——分子生物學不是一門課,而是整個生醫世界的「語言底層」。 不論你未來在做的是: 生醫工程 生物資訊 新藥研發 臨床或產業決策 你都會不斷遇到:DNA、RNA、蛋白質、調控、突變、表現量。 沒有這層理解,你聽得懂每一個字,卻抓不到真正的重點。 工程背景自學分子生物學,最容易卡關的三個地方 1️⃣ 把分子生物學當成背誦學科 工程背景的人習慣找「規則」,但分子生物學更像是一組 有條件、有例外的系統 。 2️⃣ 一開始就鑽進太多細節 如果還沒建立整體架構,就開始記轉錄因子、修飾位點,挫折感會非常高。 3️⃣ 學完卻不知

Jason Lu
1月31日讀畢需時 2 分鐘


抗體藥物偶聯體(Antibody–Drug Conjugate, ADC)完整解析|從零開始理解設計、Linker、Internalization 與新藥平台策略
這是一篇寫給「沒有 ADC 專業背景,但想真正理解 ADC 為什麼在 2020s 成為腫瘤新藥核心平台」的長篇入門+進階文章。本文會從最基本的概念講起,逐步帶你理解 ADC 的設計邏輯、工程取捨,以及為什麼這項技術會深刻影響未來十年的癌症藥物開發與產業策略。 Executive Summary 抗體藥物偶聯體(ADC) 是一種結合「抗體精準性」與「小分子藥物高毒性」的藥物設計概念。 ADC 的成功,不只取決於抗體是否找得到癌細胞,而是 抗體、linker、payload 與細胞內運輸(internalization)是否被整體設計 。 2020 年後 ADC 爆發,來自三件事同時成熟:工程技術、新世代 payload,以及大型藥廠的策略轉向。 ADC 已從「單一藥物」進化為 可複製、可擴張的腫瘤治療平台 。 一、什麼是 Antibody–Drug Conjugate (ADC)?為什麼不能只把它當成「抗體加毒藥」? 如果你是第一次接觸 ADC,可以先把它想成一個非常直覺的概念: 用抗體當導航系統,把非常毒的藥物,精準送進癌細胞裡。...

Jason Lu
1月31日讀畢需時 4 分鐘


癌症疫苗:從免疫學理論到個人化 mRNA 治療的新時代
前言:為什麼癌症疫苗重新成為焦點? 長期以來,「 癌症疫苗 」在腫瘤學中一直是一個充滿理想、卻屢遭挫折的概念。早期多數治療型癌症疫苗在臨床試驗中未能顯示明確療效,使得學界與產業界對於免疫系統是否真的能被有效「訓練」來對抗癌細胞,抱持高度懷疑的態度。 然而,這個局面正在快速改變。 隨著 腫瘤基因體定序、腫瘤新抗原(neoantigen)鑑定,以及 mRNA 傳遞技術 的成熟,癌症疫苗研究迎來了新的轉捩點。截至 2025–2026 年,已有多項 癌症疫苗臨床試驗 在黑色素瘤、肺癌、胰臟癌、大腸直腸癌等多種實體腫瘤中進行,且部分計畫已推進至後期臨床階段。更重要的是,現代癌症疫苗多半不再單獨使用,而是與 免疫檢查點抑制劑 併用,展現出新的治療潛力。 什麼是癌症疫苗? 癌症疫苗(cancer vaccine)是一種免疫治療策略,目標是誘發或增強病人自身的免疫系統,使其能夠辨識並攻擊癌細胞。與預防傳染病的疫苗不同,多數癌症疫苗屬於治療型疫苗(therapeutic vaccines) ,是在癌症已經發生後施打。 癌症疫苗的核心概念,是將 腫瘤相關抗原...

Jason Lu
1月25日讀畢需時 6 分鐘


PEG-free LNP:BioNTech 如何用電荷重新定義 mRNA 遞送的穩定性設計
前言 在 mRNA therapeutics 與 lipid nanoparticle(LNP)領域中, PEG-lipid 幾乎被視為不可或缺的標準元件 。 PEG 的角色很清楚: 提供 steric shielding,防止顆粒聚集 延長血液循環時間 降低非專一性吸附 然而,隨著 mRNA 技術從「一次性疫苗」走向「重複給藥的系統性治療」, PEG 相關的 anti-PEG 抗體 與 Accelerated Blood Clearance(ABC)現象 ,逐漸成為實際的臨床與平台風險。 BioNTech Delivery Technologies 團隊近期發表的一篇 bioRxiv 論文,提出了一個關鍵問題: LNP 的穩定性,真的只能靠 PEG 提供的 steric shielding 嗎? 他們的答案,催生了一個值得整個 delivery field 認真對待的概念: PEG-free LNP 。 為什麼 PEG-free LNP 會失穩?問題出在 pH 7.4 這篇論文的價值,不在於「去掉 PEG」,而在於 先釐清問題本身 。 作者首

Jason Lu
1月23日讀畢需時 4 分鐘

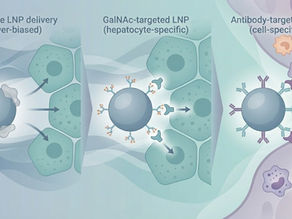
Targeted LNP Delivery:從 GalNAc 到抗體導向的下一代核酸遞送策略
前言:LNP 的下一個瓶頸,不是包得進去,而是「送對地方」 脂質奈米粒子(Lipid Nanoparticles, LNPs)已成功支撐 mRNA 疫苗與多項核酸藥物上市,證明其在體內遞送脆弱核酸分子的可行性。然而,隨著適應症從肝臟擴展至免疫細胞、中樞神經系統與實體腫瘤, 「非專一性體內分佈」正逐漸成為 LNP 發展的主要限制 。 對多數 LNP 平台而言,問題已不再是「能不能表現」,而是: 是否需要過高劑量才能達到目標組織 是否造成不必要的 off-target exposure 是否壓縮了治療指數(therapeutic window) 在這樣的背景下, targeted LNP delivery(目標導向式 LNP 遞送) 成為下一代核酸藥物平台的關鍵戰場。 為什麼多數 LNP 會「自然地」累積在肝臟? 在討論 targeted LNP 之前,有一個基本事實必須先釐清: 多數系統性給藥的 LNP,並非「被設計送去肝臟」,而是「被生物系統帶去肝臟」。 LNP 進入體循環後,會快速吸附血清蛋白,特別是 apolipoprotein E(Apo

Jason Lu
1月18日讀畢需時 4 分鐘


實驗設計(DoE):原則、優勢與對科學研發的關鍵影響
前言:當研發問題不再只靠「多做幾組實驗」 在現代科學研究與工程研發中,真正的挑戰早已不是「要不要做實驗」,而是—— 如何在有限的時間、資源與樣本數下,系統性地理解複雜系統,並做出正確決策。 無論是在藥物開發、製程優化、材料工程,或生醫平台研發中,研究人員往往同時面對多個可調變因。若仍採用傳統的一次只改一個變因(One-Factor-at-a-Time, OFAT)方法,不僅效率低落,也極容易錯失關鍵的交互作用(interaction)。 實驗設計(Design of Experiment, DoE) 正是在這樣的背景下,成為現代研發不可或缺的核心方法。 什麼是實驗設計(DoE)? 實驗設計(DoE)是一套以統計為基礎的方法論,用來系統性地研究多個輸入變因(factors)如何同時影響一個或多個輸出結果(responses)。 DoE 的核心精神不在於「做更多實驗」,而在於: 用最少、最有策略的實驗,獲得最大資訊量,並建立可解釋、可預測的模型。 這對於高度多變、非線性、且存在交互作用的系統尤其重要。 實驗設計(DoE)的四大核心原則 1️⃣ 隨機

Jason Lu
1月18日讀畢需時 4 分鐘


高通量 LNP 篩選技術:條碼化(Barcoding)如何改變脂質奈米粒子研發
前言:核酸藥物真正的瓶頸,其實在「遞送」 mRNA 疫苗、siRNA 藥物、CRISPR 基因編輯等核酸藥物,已經徹底改變了現代醫療。然而,這些療法能否真正成功,關鍵往往不只在於「序列設計」,而是在於—— 核酸能不能被有效、安全且精準地送到正確的細胞與器官 。 脂質奈米粒子(Lipid Nanoparticles, LNPs)目前仍是核酸藥物體內遞送的主流平台。透過包覆脆弱的核酸分子、避免體內降解,並促進細胞吸收,LNP 技術促成了 Onpattro® 、 Comirnaty® 與 Spikevax® 等關鍵產品的成功。 但 LNP 的設計本質上是一個高度多變、難以直覺優化的工程問題 。 離子化脂質的化學結構、脂質比例、PEG 密度、脂肪酸尾端設計,只要稍有不同,就可能徹底改變: 體內分佈(biodistribution) 轉染效率 免疫反應與毒性輪廓 過去,LNP 的篩選大多仰賴「一種配方對應一隻動物」的方式,搭配螢光或 luciferase reporter。這樣的流程不僅成本高、耗時長,也嚴重限制了可探索的配方空間。 近年來, DNA

Jason Lu
1月18日讀畢需時 5 分鐘


工程背景是跨領域學習的優勢,還是包袱?給想走向生醫的你
前言 在跨領域學習的過程中,「工程背景」究竟是優勢,還是反而成為進入生醫與生命科學的包袱?這篇文章將結合我自身從工程跨入生醫工程、分子生物與生物資訊的經驗,深入解析工程背景在 跨領域學習 中的實際影響。 很多工程背景的人,其實都有同一個焦慮 如果你是工程背景,卻對生醫、生命科學或其他領域感到興趣,你可能也曾經問過自己: 我是不是永遠不夠「像生物人」? 我的工程訓練,會不會反而成為跨領域學習的阻礙? 我到底該保留哪些能力,又該放下什麼? 這些焦慮其實非常普遍,而且合理。因為跨領域學習,本來就不是把一套能力直接搬到另一個領域。 工程背景在跨領域學習中的三個隱性優勢 在我實際從工程走向生醫工程、分子生物與生物資訊的過程中,我逐漸發現,工程背景並不是劣勢,而是 需要被正確使用的優勢 。 1️⃣ 問題拆解能力 工程訓練讓人習慣先問:「問題是什麼?」 在跨領域學習時,這讓我能夠快速判斷: 目前真正卡關的是概念?技術?還是資料? 哪些知識是現在必須補的,哪些可以之後再說? 2️⃣ 系統性思考 工程背景讓我不會只盯著單一結果,而是去理解整個系統如何運作。...

Jason Lu
1月14日讀畢需時 3 分鐘


跨領域不是天賦:我如何靠自學,從工程一路走到生醫與生物資訊
跨領域學習不是天賦:我如何靠自學,從工程一路走到生醫與生物資訊 跨領域學習的起點:我不是一開始就走在「對的路」上 很多人以為我一路都在做生醫相關的研究,但事實上,我的起點是工程—— 化學工程與土木工程 。那時候的我,對生物的理解非常有限,更不用說分子層級的調控機制、細胞訊號傳遞,或是後來成為日常的生物資料分析。 工程背景給我的,並不是「比較聰明」,而是一種習慣: 遇到問題先拆解,而不是先害怕 。但老實說,剛跨進生醫領域時,我其實非常不安,因為我很清楚自己在「基礎知識」上落後同儕一大截。 那段時間,我很早就意識到一件事:如果我想走得下去,靠的只會是 持續而有策略的自學 。 跨領域學習的第一關:工程訓練教會我解題,卻沒教我如何面對生命的複雜 工程訓練讓我很自然地去做這些事: 清楚定義問題 建立可驗證的假設 用模型或流程簡化系統 但真正進入生醫領域後,我很快發現這套思維有它的極限。生命系統充滿例外、變異與噪音,很多時候你無法用一個漂亮的模型解釋所有現象。 跨領域真正困難的地方,不是學新知識,而是放下舊有的確定感。 我第一次深刻體會到: 跨領域不是能力的

Jason Lu
1月12日讀畢需時 3 分鐘


脂質奈米粒子如何實現先進核酸遞送:LNP 藥物遞送(LNP drug delivery)的工程原理解析
前言:脂質奈米粒子在核酸治療中的關鍵角色 在過去十年間, 脂質奈米粒子(lipid nanoparticles, LNPs) 已成為核酸治療(nucleic acid therapeutics)中最關鍵的遞送技術之一,支撐了多項臨床與商業化成功案例,包括 Onpattro®(patisiran) 以及 Pfizer-BioNTech 與 Moderna 的 mRNA COVID-19 疫苗。 雖然核酸藥物常被聚焦於序列設計或分子生物學層面,但在真實世界中, 治療成效往往取決於遞送系統本身是否被正確工程化 。 LNP 藥物遞送(LNP drug delivery)並非被動載體,而是一個高度可設計的工程系統 ,其脂質組成、電荷行為與結構動態,直接決定體內分佈、細胞攝取、內涵體逃脫(endosomal escape),以及最終的臨床表現。 本文將從工程與平台設計的角度,解析 LNP 藥物遞送的核心設計原理 ,說明脂質組成如何形塑核酸治療的效率、安全性與可預測性。 脂質奈米粒子的基本組成:LNP 的四大核心元件 大多數臨床級 LNP 藥物遞送系統,由

Jason Lu
1月11日讀畢需時 4 分鐘


精通 mRNA 合成(mRNA synthesis):從體外轉錄、5′ 端加帽到 Poly(A) 尾端工程的完整解析
前言 信使核醣核酸(messenger RNA, mRNA)已徹底改變現代醫療的可能性。作為一種治療平台,mRNA 使疫苗能夠快速開發,也推動了個人化癌症免疫治療與罕見疾病的蛋白質替代策略。然而,每一項成功的 mRNA 治療產品背後,都仰賴一套 高度工程化的 mRNA 合成流程 。 在多數討論中,mRNA 治療(mRNA therapeutics)的臨床成果往往成為焦點,但實際上, mRNA 合成(mRNA synthesis)的品質,才是真正決定轉譯效率、免疫反應、製程可擴展性與法規可行性的關鍵 。體外轉錄(IVT)、5′ 端加帽(5′ capping)與 Poly(A) 尾端工程中的每一個決策,都會直接影響一個 mRNA 產品能否從實驗室順利推進至臨床與量產。 本文將以工程與 CMC(Chemistry, Manufacturing, and Controls)的視角,深入解析 mRNA 合成 的三大核心模組: 體外轉錄(In Vitro Transcription, IVT) 5′ 端加帽策略 Poly(A) 尾端工程 這三者共同構成現代

Jason Lu
1月11日讀畢需時 4 分鐘
bottom of page