top of page
盧創
工作室


讓創意落地,發揮影響力
將深度科學、商業洞察與職涯策略,轉化為清楚且可執行的下一步。
All Posts

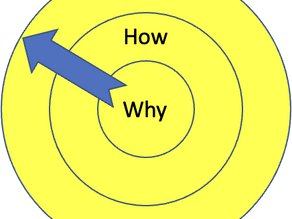
領導力系列(四):Golden Circle Leadership:為什麼真正有影響力的領導者,都是從「Why」開始
前言:領導力,不只是方向,而是意義 在前幾篇文章中,我談到了日常領導力、自我覺察,以及人格特質。 但在這些之上,還有一個更關鍵的層次,決定了一個人是否只是「能帶人做事」,還是真正能「帶人走得遠」: 👉 是否能賦予事情意義。 大多數領導者可以分配任務。有些領導者可以制定策略。 但只有少數人,能讓團隊真正相信他們正在做的事情。 這正是 Simon Sinek 提出的 Golden Circle Theory 的價值所在—— 它不只是溝通技巧,而是一種領導的思考框架(leadership operating system)。 Golden Circle Leadership:一個簡單但改變本質的模型 Golden Circle 分成三層: Why(為什麼):目的、信念、存在的理由 How(怎麼做):方法、策略、執行方式 What(做什麼):產品、結果、產出 大多數組織與領導者的溝通方式是: What → How → Why(由外而內) 但真正有影響力的領導者,則是反過來: Why → How → What(由內而外) 這看起來只是順序上的差異。 但本

Jason Lu
5天前讀畢需時 5 分鐘

Teplizumab for Type 1 Diabetes:我們第一次開始改變疾病進程
前言:治療,第一次不只是控制血糖 長期以來,第一型糖尿病(Type 1 Diabetes, T1D)的治療其實很單純。 身體無法製造 insulin,我們就補充 insulin。 這個方法有效,但如果再往下問一層,很快會發現一件事: 我們並沒有真正改變疾病本身。 問題不只是 insulin 不夠,而是免疫系統正在持續破壞 β 細胞。 因此,一個新的問題開始出現: 我們能不能改變 Type 1 Diabetes 的疾病進程? Tzield(teplizumab)就是在這個問題下誕生的。 一、Tzield 是什麼?(Teplizumab for Type 1 Diabetes overview) Tzield(teplizumab)是一種: anti-CD3 monoclonal antibody 與傳統治療不同,它的目標不是 β 細胞,而是免疫系統本身。 用一個直覺理解 如果第一型糖尿病的問題是: 免疫系統攻擊 β 細胞 那 Tzield 做的事情是: 讓免疫系統降低攻擊強度 不是關閉免疫系統,而是調整它的狀態。 二、為什麼這是一個重要轉變...

Jason Lu
6天前讀畢需時 3 分鐘


免疫系統是怎麼開始攻擊 β 細胞的?從直覺理解到 Type 1 Diabetes autoimmune mechanism
前言:這不是一個「突然發生」的疾病 大多數人對第一型糖尿病(Type 1 Diabetes, T1D)的理解是某一天發病,然後開始依賴 insulin。 但從生物學的角度來看,這個疾病更像是一個長時間累積的過程,可能持續數年,甚至更久。 這背後的核心,其實是 Type 1 Diabetes autoimmune mechanism 的逐步失衡。 問題從來不是單純的血糖,而是免疫系統在什麼時候開始做出錯誤的判斷。 一、先用一個直覺理解:免疫系統出錯了(Type 1 Diabetes autoimmune mechanism) 可以把免疫系統想成一個安全系統。 它的任務是辨識自己(self)與外來(non-self),並對外來威脅做出反應。 在正常情況下,它會攻擊病毒,同時保護身體自己的細胞。 但在第一型糖尿病中,這個系統開始出現誤判。 它把本來應該被保護的 β 細胞,當成需要被清除的目標。 這就是 Type 1 Diabetes autoimmune mechanism 的起點。 二、為什麼會誤判?三個關鍵因素 這個錯誤不是單一事件,而是多個因素逐

Jason Lu
4月26日讀畢需時 4 分鐘


第一型糖尿病(Type 1 Diabetes):當免疫系統開始誤判自己,我們其實在對抗的是什麼?
前言:問題從來就不只是血糖 如果你真的接觸過第一型糖尿病(T1D),很快就會發現一件事: 「血糖失控」只是最後的結果 真正的問題,是更深層的系統錯誤—— 免疫系統開始攻擊自己 這也是為什麼,過去 100 年我們雖然能用 insulin 控制疾病,卻始終沒有真正「解決」它。 一、第一型糖尿病是什麼?(Type 1 Diabetes overview) 第一型糖尿病本質上是一種自體免疫疾病。 免疫系統中的 T 細胞錯誤地辨識胰臟中的 β 細胞(負責分泌 insulin),並持續將其破壞,最終導致: insulin 無法分泌 血糖失控 必須終身依賴外源性 insulin 所以真正的問題不是「insulin 不夠 而是「製造 insulin 的細胞被消滅了」 二、第一型糖尿病的原因:基因 × 環境 × 免疫失衡 基因只是風險,不是命運 T1D 與 HLA(human leukocyte antigen)基因高度相關,但: 同卵雙胞胎一致率只有約 30–50% 代表:基因只是背景,真正的 trigger 在環境 環境因素:真正啟動疾病的開關 近年最一致的

Jason Lu
4月25日讀畢需時 4 分鐘


B Cell Protein Factory:HSPC 基因編輯如何把 B 細胞變成長效治療蛋白工廠?
Executive Summary B cell protein factory 是一種新型 biologics delivery 模式 透過 HSPC gene editing ,讓 B 細胞長期分泌抗體或治療蛋白 系統具備 可放大(boostable)、可持續(long-term)、可多蛋白(multi-output) 的特性 代表 cell therapy 從「殺細胞」走向「生產蛋白」的轉變 Be Biopharma、Immusoft 等公司已開始布局類似方向 前言:我們是否正在重新定義 biologics? B cell protein factory 正在成為下一代生技平台中一個非常值得關注的方向。 在過去的 biologics 世界裡,我們習慣的模式是: 設計蛋白或抗體 製造 注射 維持血中濃度 這是一個成熟但本質上仍然是: 👉 外加型藥物(exogenous delivery) 但現在,一個新的思考正在出現: 👉 如果人體可以自己持續生產藥物呢? 最新研究顯示,透過 HSPC gene editing ,我們可能可以把 B

Jason Lu
4月19日讀畢需時 4 分鐘


Digital Twin in Biotech:從製程優化到臨床試驗的下一個操作系統
前言:我們真的開始「理解」生物系統了嗎? 在過去的生技產業裡,我們其實很少真正「理解」系統。 我們做的更多是: 做實驗 看結果 再調整 這種方式有效,但本質上仍然是 trial-and-error driven science 。 而 Digital Twin in Biotech 的出現,代表一個本質上的轉變: 我們開始嘗試在「實驗之前」,先理解系統。 這不只是效率的提升,而是整個 biotech 產業思維的升級。 What is Digital Twin in Biotech?不只是模型,而是系統 Digital Twin(數位分身)的核心概念是: 一個能夠動態反映真實系統的「虛擬對應體」 在 biopharma 中,它通常包含: 機制模型(mechanistic modeling) AI / machine learning 模型 即時數據(PAT sensors) 多尺度整合(cell → process → patient) 更精確地說,它是一個: 能整合 biological mechanism、process parameters

Jason Lu
4月18日讀畢需時 4 分鐘


Antibody Drug Conjugates (ADC) Ultimate Guide:從分子設計到臨床開發、製造與市場策略
Executive Summary 抗體藥物偶聯體(Antibody Drug Conjugates, ADCs)已成為近年腫瘤治療與生醫產業中最重要的創新之一。 在過去十年中, antibody drug conjugates 已從早期研究技術,發展為橫跨科學、臨床、製造與市場的整合性系統。 單純從分子設計或臨床療效理解 ADC,已無法完整掌握這個領域。 Antibody drug conjugates 是一個結合 biology、chemistry、engineering 與 strategy 的跨領域系統 本篇《ADC Ultimate Guide》將完整解析: ADC design 與 ADC mechanism ADC clinical development ADC manufacturing(CMC) ADC market 與產業策略 一、什麼是 Antibody Drug Conjugates(ADC)? Antibody drug conjugates(抗體藥物偶聯體)的核心概念是: 👉 利用抗體將高毒性藥物精準傳遞至腫瘤細

Jason Lu
4月12日讀畢需時 3 分鐘


mRNA folding 新視角:從結構與熱力學,重新理解 RNA delivery 的瓶頸
前言:我們是不是一直忽略了最關鍵的東西? 這幾年 mRNA therapeutics 很熱,從疫苗一路延伸到癌症、基因編輯、蛋白補充。 但如果你有實際做過這一塊,應該都會有一個很直覺的感受: 很多時候,不是你設計不夠好,而是 delivery 上不去。 於是大家開始優化: codon nucleoside modification cap / polyA LNP 配方 這些當然都重要,但本質上都還是在同一個框架裡: 👉 我們把 mRNA 當成一條「序列」在優化 但這篇 Nature Nanotechnology 的工作,某種程度是在提醒我們: mRNA 其實是一個有「形狀」的分子。 一個簡單但很關鍵的想法:把 mRNA 折起來 (mRNA folding) 這篇 paper 提出一個策略: 用金屬離子,把 mRNA「折」起來(MARF) 不是改 sequence,也不是改 lipid,而是: 👉 直接改 mRNA 的三維結構 結果很直接: protein expression 提升最高 7.3 倍 in vivo 表現也同步提升 CRI

Jason Lu
4月11日讀畢需時 4 分鐘

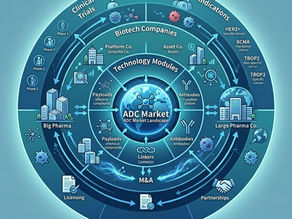
ADC 系列(十)ADC 市場(ADC market)與策略:抗體藥物偶聯體如何改變生醫產業競爭格局
Executive Summary 抗體藥物偶聯體(Antibody–Drug Conjugates, ADCs)已從一項創新治療技術,快速發展為生醫產業中最受關注的戰略領域之一。 近年來, ADC market 出現明顯變化: 大量授權(licensing)與併購(M&A)交易 大藥廠積極建立 ADC pipeline 新創公司專注於 ADC platform 技術 這些現象顯示: ADC market 已成為 oncology 領域中最活躍、最具競爭性的產業板塊之一 本篇文章將解析: 為什麼 ADC market 成為產業熱點 大藥廠與新創的策略差異 ADC pipeline 的競爭邏輯 2023–2026 的市場與交易趨勢 未來 ADC 的產業發展方向 一、為什麼 ADC market 成為熱門領域? 1️⃣ 臨床成功建立市場信心 近年 ADC 的成功案例: Enhertu(trastuzumab deruxtecan) Trodelvy 顯示 ADC 已具備: 強效抗腫瘤能力 可擴展適應症 👉 這些成功案例直接推動 ADC marke

Jason Lu
4月5日讀畢需時 3 分鐘


ADC 系列(九)ADC Manufacturing & CMC:抗體藥物偶聯體如何從實驗室走向量產?
Executive Summary 抗體藥物偶聯體(Antibody–Drug Conjugates, ADCs)不僅在科學與臨床上具有高度潛力,在製造層面也極具挑戰。 與傳統抗體或小分子藥物相比,ADC 的製造涉及: biologics(抗體) highly potent small molecules(payload) 複雜的 conjugation chemistry 因此, ADC manufacturing 與 CMC(Chemistry, Manufacturing, and Controls) 往往成為產品開發中的關鍵瓶頸。 許多 ADC: 科學上合理 臨床上有訊號 卻卡在 scale-up 或品質一致性 本篇文章將解析: ADC 的製造流程 DAR(Drug-to-Antibody Ratio)控制 conjugation engineering scale-up 與 GMP 挑戰 為什麼 CMC 常成為開發瓶頸 一、什麼是 ADC 的 CMC? CMC(Chemistry, Manufacturing, and...

Jason Lu
3月29日讀畢需時 3 分鐘


In vivo CAR-T Therapy最新臨床突破:從細胞製造到體內編程的革命
前言:CAR-T 的下一步,不只是更好,而是更簡單 過去十年,CAR-T therapy 已經證明我們可以用工程化免疫細胞治療癌症。 但真正的瓶頸從來不是 efficacy,而是: 成本太高 製程太慢 病人等不起 傳統 CAR-T 的本質,其實是「個人化細胞製造」。 而現在,一個更根本的問題出現了: 如果 CAR-T 根本不需要製造呢? 這就是最新臨床研究所揭示的方向: in vivo CAR-T therapy 技術本質:把人體變成 CAR-T 的製造工廠 傳統 CAR-T(ex vivo CAR-T)的流程,本質上是一個「個人化細胞製造」: Leukapheresis(白血球分離) → 從患者體內收集周邊血單核細胞(peripheral blood mononuclear cells, PBMCs),並分離出 T 細胞 Ex vivo gene engineering(體外基因工程) → 通常使用 lentiviral 或 retroviral vector 將 CAR 基因導入 T 細胞 Cell expansion(細胞擴增)...

Jason Lu
3月28日讀畢需時 5 分鐘


ADC 系列(八)ADC Clinical Development Strategy:抗體藥物偶聯體如何走到臨床成功?
Executive Summary- ADC clinical development 抗體藥物偶聯體(Antibody–Drug Conjugates, ADCs)在工程與科學層面已取得重大進展,但臨床成功率仍然具有高度不確定性。 許多 ADC: 在 preclinical 模型中表現優異 在早期臨床試驗(Phase I)顯示反應 卻在 Phase II / III 試驗失敗 這代表問題不只是分子設計,而是: ADC clinical development strategy(臨床開發策略) 成功的 ADC 通常同時做到: 正確的劑量與給藥策略 精準的病人選擇(patient selection) 可控的毒性(toxicity profile) 合理的法規與臨床路徑(regulatory strategy) 本篇文章將系統性解析這些關鍵因素。 一、ADC 的臨床失敗通常發生在哪裡? 很多 ADC 並不是「完全無效」,而是: efficacy 不穩定 toxicity 無法接受 trial 設計無法證明 benefit 常見情境包括: Phase

Jason Lu
3月22日讀畢需時 4 分鐘


In Vivo CAR-T 自體免疫療法:開創免疫治療新前沿
In Vivo CAR-T 自體免疫療法:在體內重塑免疫系統 前言 CAR-T 療法已徹底改變血液腫瘤治療格局。然而,其拓展至自體免疫疾病的應用,仍受限於高昂成本、製程複雜度,以及難以規模化生產等挑戰。 如今,一種新的典範正在形成: in vivo CAR-T 自體免疫療法 。 不同於將 T 細胞取出體外改造、培養數週後再回輸體內,in vivo 策略是在患者體內直接編程免疫細胞,使人體本身成為製造場域。 對於自體免疫疾病而言——其治療目標是「免疫重置」而非腫瘤清除——這種差異可能具有決定性意義。 什麼是 In Vivo CAR-T? 傳統(ex vivo)CAR-T 療法流程包括: 白血球分離術(Leukapheresis) 病毒載體基因轉殖 細胞體外擴增 品質控制檢測 回輸患者體內 相較之下, in vivo CAR-T 自體免疫療法 是透過病毒載體或標靶奈米顆粒,將編碼 CAR 的遺傳物質(mRNA 或 DNA)直接送入體內循環中的 T 細胞。 這種概念轉變看似簡單,卻極具顛覆性: 從體外製造細胞 轉向在體內重新編程免疫系統。 這使 CAR

Jason Lu
3月21日讀畢需時 6 分鐘


ADC 系列(七)Next-Generation ADC Platforms:下一代抗體藥物偶聯體正在如何被設計?
Executive Summary 抗體藥物偶聯體(ADC)在過去十年已成為腫瘤治療的重要藥物類型。 然而,第一代與第二代 ADC 的設計仍然存在限制,例如: 單一 payload 機制 單一 target 分子工程彈性有限 因此,許多研究團隊開始重新思考: 如果 ADC 不只是「抗體+毒藥」,而是一個可工程化的平台呢? 這篇文章將介紹 next-generation ADC platforms 的主要方向,包括: dual-payload ADC bispecific ADC payload engineering tumor-selective linker design targeted delivery platforms 這些新策略正在重新定義 ADC 的未來。 一、為什麼需要 Next-Generation ADC? 早期 ADC 的設計通常比較簡單: 單一 monoclonal antibody 單一 payload 傳統 linker 然而腫瘤生物學的複雜性意味著: tumor heterogeneity adaptive re

Jason Lu
3月15日讀畢需時 2 分鐘


mRNA-LNP Stability:RNA藥物成功背後最困難的工程挑戰
前言 在 COVID-19 疫苗成功之後, mRNA 技術迅速成為生醫領域最重要的藥物平台之一 。 透過讓人體細胞暫時表達特定蛋白質,mRNA therapeutics 正被應用於多種醫療領域,例如: 疫苗 癌症免疫治療 蛋白質替代療法 基因編輯(CRISPR delivery) 然而,mRNA 本身極其脆弱。 如果沒有保護機制,mRNA 在體內幾乎會在短時間內被降解。因此所有 mRNA 藥物都依賴一種關鍵技術: Lipid Nanoparticles (LNPs) 。 這些奈米顆粒能夠包覆 RNA,並將其安全地送入細胞。 但這項技術同時帶來了一個巨大的挑戰: mRNA-LNP 的穩定性非常複雜。 近期一項研究系統性分析了不同配方與儲存條件對 mRNA-LNP 長期穩定性的影響,並揭示了影響 RNA 藥物 shelf-life 的關鍵因素。 mRNA- LNP 的基本結構 要理解為什麼 mRNA-LNP stability 如此具有挑戰性,我們需要先了解這種奈米遞送系統的基本組成。 典型的 mRNA-LNP 由四種主要脂質組成: Ioniz

Jason Lu
3月14日讀畢需時 5 分鐘


ADC 系列(六)ADC Combination Therapy:為什麼抗體藥物偶聯體幾乎都需要合併療法?
Executive Summary 抗體藥物偶聯體(Antibody–Drug Conjugates, ADCs)在過去十年間已成為腫瘤藥物開發的重要平台。然而,即使是臨床上表現非常成功的 ADC,也很少能長期單獨控制腫瘤。 原因在於腫瘤具有高度適應能力。腫瘤細胞可以透過多種機制逐漸逃避 ADC 的攻擊,例如抗原下降、內吞效率改變、或 DNA repair pathway 的補償。 因此,越來越多研究開始探索 ADC combination therapy ,也就是將 ADC 與其他抗癌策略結合,例如免疫療法、小分子標靶藥物或 DNA repair 抑制劑。 這篇文章將解析: 為什麼單一 ADC 很難長期控制腫瘤 ADC 與免疫療法的機制協同 ADC 與 DNA repair 抑制劑的潛在組合 Multispecific ADC 的未來方向 Combination therapy 的臨床試驗 landscape 理解這些概念,有助於從單一藥物開發轉向 平台級策略設計 。 一、為什麼單一 ADC 很難長期控制腫瘤? 在前一篇文章中,我們討論了 AD

Jason Lu
3月7日讀畢需時 4 分鐘


ADC 系列(五)ADC Resistance:為什麼抗體藥物偶聯體會失效?
文章定位 這是 ADC 系列第五篇。 在前幾篇中,我們談了: ADC 系統設計 Linker 與 conjugation Target selection 臨床轉譯與產業價值 這一篇要面對一個更現實的問題: 即使設計合理、臨床成功,為什麼 ADC resistance 仍然不可避免? Executive Summary ADC resistance 是多機制共同作用的結果。 抗原下降與異質性會降低藥物進入效率。 Internalization 與 lysosomal trafficking 改變會減少 payload 釋放。 ABC transporters 可能將 payload 排出細胞。 DNA damage response 與細胞適應機制降低毒性效果。 下一代 ADC 正透過 dual payload、multispecific 與新機制 payload 來延緩抗藥性。 一、Target Downregulation 與抗原異質性 最直觀的 ADC resistance 機制是: 抗原表現下降 抗原基因變異 腫瘤內部高度異質性 當抗原密

Jason Lu
2月22日讀畢需時 3 分鐘


ADC 系列(四)ADC Target Selection:哪些抗原真正適合抗體藥物偶聯體?
前言 這是 ADC 系列的第四篇文章。 如果前幾篇我們談的是: ADC 是一個整合系統(Series 一) 為什麼 2020 年後 ADC 進入成熟期(Series 二) Linker 與 Conjugation 的工程核心(Series 三) 那麼這一篇將往更上游走一步,回答一個根本問題: ADC target selection:哪些抗原真的適合做 ADC? 這篇文章寫給沒有 ADC 背景,但希望從第一原理理解「生物學條件如何決定藥物上限」的讀者。 Executive Summary | ADC target selection ADC target selection 是整個專案的第一個、也是最難修正的決策。 高表現抗原不等於適合 ADC,internalization 才是關鍵。 抗原密度、腫瘤異質性與正常組織表現,直接決定療效與毒性風險。 Antigen shedding 可能成為隱性藥物黑洞(antigen sink)。 Multispecific ADC 提供新方向,但同時提高設計門檻。 一、ADC 為什麼不是所有腫瘤標的的萬用解?

Jason Lu
2月14日讀畢需時 4 分鐘


LNPDB是什麼?從資料庫到 AI 與分子動力學,重新理解脂質奈米粒的設計邏輯
前言 為什麼 LNP 領域,一直缺一個「PDB 等級」的資料庫? 如果你實際參與過 mRNA、siRNA 或 CRISPR 的 lipid nanoparticle(LNP)設計,你很可能有這樣的感覺: 我們其實做了非常多 LNP screening,但這些資料始終無法真正「累積成知識」。 LNP 領域長期存在一個結構性的問題: 資料很多,但高度分散;實驗成功,但難以歸納。 不同研究使用不同配方、不同 readout、不同實驗條件,使得資料難以跨研究比較或重複使用。 與蛋白質工程不同,LNP 設計至今沒有一個像 Protein Data Bank(PDB) 那樣的中央化基礎建設,能夠系統性整理「結構 × 配方 × 功能」之間的關係。這也直接限制了 AI 模型與理性化設計的發展。 LNPDB 是什麼?Lipid Nanoparticle Database 作為公共資料基礎建設 Lipid Nanoparticle Database(LNPDB) https://lnpdb.molcube.com/ LNPDB 是由 MIT(Dr. Daniel

Jason Lu
2月8日讀畢需時 3 分鐘


ADC 系列(三)Linker 與 Conjugation:ADC 真正的工程核心,為什麼多數團隊低估了它?
前言 這是 ADC 系列的第三篇文章,寫給 沒有化學或 ADC 工程背景 ,但想真正理解: 為什麼很多 ADC 專案「看起來都合理」,最後卻在臨床或放大製程中失敗? 本篇將聚焦在 linker 與 conjugation strategy —— 這兩個最常被視為「技術細節」,卻最常成為 結構性失敗來源 的關鍵設計。 Executive Summary 如果你只記得一件事: ADC 的成敗,往往不是輸在抗體或 payload,而是輸在 linker 與偶聯策略。 因為 linker 與 conjugation 決定的不是「藥有多毒」, 而是: 毒藥什麼時候釋放 在哪裡釋放 有多少分子真的能照設計行事 一、為什麼 Linker 是 ADC 最被低估的元件? 在許多入門介紹中,linker 常被一句話帶過: 「linker 是把抗體和藥物接起來的化學結構。」 但在實際開發中,linker 解決的是一個 極度困難的工程問題 : 如何讓 ADC 在血液中穩定數天,卻能在癌細胞內準確釋放 payload? 這意味著 linker 必須同時滿足三個互相衝突的

Jason Lu
2月7日讀畢需時 4 分鐘
bottom of page